| Themen-Auswahl | ENERGIE-WISSEN | Leitseite |

|
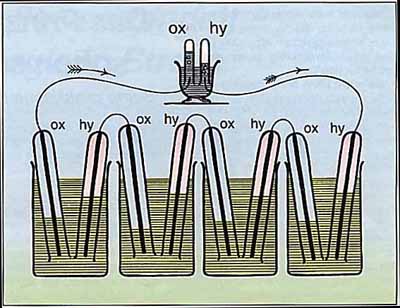
Diese Brennstoffzelle hat vor über 150 Jahren der Engländer Grove aus vier hintereinander geschalteten Elementen konstruiert: In jedem der vier Gefäße befindet sich verdünnte Schwefelsäure, in die zwei Glasröhren mit Elektroden aus Platin eintauchen. Im oberen Teil der Glasröhren werden die Anoden von Wasserstoff (hy)und die Kathoden von Sauerstoff (ox) umspült. Der erzeugte Strom speist auf dieser Abbildung einen Elektrolyseur. (Aus: W. Ostwald, Elektrochemie, Leipzig 1896) |
Wie schon erwähnt, ist die Brennstoffzelle als galvanisches Element mit der Batterie verwandt. Noch enger ist die Verwandtschaft zur Elektrolyse: Bei diesem elektrochemischen Prozeß wird Gleichstrom durch Wasser geleitet, wodurch sich am negativen Pol Wasserstoff und am positiven Pol Sauerstoff bildet. Die Enden der beiden metallischen Leiter, die in die Flüssigkeit eintauchen, nennt man Elektroden. Stülpt man über diese Elektroden jeweils ein Glasröhrchen, kann man die erzeugten Gase darin auffangen. Wenn man den Inhalt der beiden Röhrchen zusammenbringt, entsteht aus Wasserstoff und Sauerstoff ein Gemisch, das explosionsartig verbrennt und als "Knallgas" bezeichnet wird.
Im Unterschied zur Elektrolyse funktioniert aber die Brennstoffzelle (die früher auch als "Knallgas-Zelle" bezeichnet wurde) genau umgekehrt: Hier wird nicht mit Strom Wasserstoff und Sauerstoff erzeugt, sondern es wird mittels Wasserstoff und Sauerstoff elektrische Energie gewonnen. Es wird also gegenüber der Elektrolyse die Richtung der Energieumwandlung vertauscht, ähnlich wie bei einem elektrischen Motor, der normalerweise Strom in mechanische Energie umwandelt, aber genauso als Generator bzw. Stromerzeuger dienen kann, wenn man ihn mit mechanischer Energie antreibt. In der Praxis ist die Umkehrung der Energieumwandlung bei der Elektrolyse allerdings nicht so einfach wie beim elektrischen Motor, wie wir noch sehen werden.

|
Sir William Robert Grove (1811 - 1896) konstruierte schon 1839 die erste Brennstoffzelle. |
Die erste Brennstoffzelle wurde schon 1839 von dem Engländer Sir William Grove konstruiert. Ihre Weiterentwicklung zu einer tatsächlich leistungsfähigen Stromquelle erwies sich jedoch als derart schwierig, daß Groves Konzept fast ein Jahrhundert lang nicht weiter verfolgt wurde. Hinzu kam, daß 1866 mit der Entdeckung des dynamoelektrischen Prinzips eine Stromquelle gefunden wurde, mit der jede Art mechanischer Energie in beliebiger Menge und höchst effizient in Strom verwandelt werden konnte. Die Batterien verloren ihre bisherige Bedeutung als einzige praktisch verwertbare Stromquelle und konnten sich mit ihren bescheidenen Leistungen nur noch in Nischen behaupten. Das von Grove entwickelte Konzept der Brennstoffzelle bekam nicht einmal diese Chance, sondern verstaubte in den Lehrbüchern über galvanische Elemente.
Groves Brennstoffzellen hatten Elektroden aus Platin, die innerhalb eines Glasröhrchens mit dem unteren Teil in verdünnte Schwefelsäure als Elektrolyt eintauchten, während sie im oberen Teil des Glasröhrchens von Wasserstoff bzw. Sauerstoff umspült wurden. Das reichte, um eine Spannung von etwa einem Volt zu erzeugen. Man konnte sie nachweisen, wenn man ein Meßinstrument an die beiden Elektroden anschloß.
Ein ähnlicher Effekt ließ sich bei der Elektrolyse von Wasser beobachten, wenn man die Stromquelle schnell durch ein Meßinstrument ersetzte, solange die beiden Elektroden noch von dem soeben erzeugten Wasserstoff bzw. Sauerstoff umspült wurden: Die Elektrolyse verlief dann einen Moment lang rückwärts und erzeugte einen Strom entgegengesetzter Richtung.

|
Michael Faraday (1791 - 1867) erklärte die Stromleitung im Wasser mittels der "Ionen" und prägte auch andere grundlegende Begriffe wie Elektrolyt, Elektrode, Kathode und Anode. |
Um aus der Brennstoffzelle eine wirklich leistungsfähige und dauerhafte Stromquelle zu machen, bedurfte es noch erheblicher technischer Anstrengungen. Der Erfolg dieser Anstrengungen hing wiederum davon ab, wieweit es gelang, die elektrochemischen Vorgänge zu verstehen, welche die Energieumwandlung bei der Elektrolyse bzw. den umgekehrten Prozeß in der Brennstoffzelle bewirken.
Da war zunächst einmal das erstaunliche Phänomen, daß Strom nicht nur durch Drähte aus Metall geleitet werden konnte, sondern auch durch Wasser, salzhaltige Lösungen und Schmelzen. Man erkannte, daß es sich dabei um eine andere Art der elektrischen Leitung als in Metallen handeln mußte. Vorläufig unklar blieb jedoch, auf welche Weise der Elektrolyt den Strom leitet, weshalb der Strom bei der Elektrolyse den Elektrolyten zerlegt oder weshalb es zu Abscheidungen an den Elektroden kommt.
Zunächst nahm man an, daß die Moleküle des Elektrolyten durch die Kraft des elektrischen Stroms gewissermaßen zerrissen würden, so daß jedes Molekül in zwei Teile zerfällt, von denen das eine positiv und das andere negativ geladen ist. Für diese Bruchstücke, die sich dann unter dem Einfluß der elektrischen Spannung zur gegensätzlich gepolten Elektrode bewegen, prägte der englische Physiker Michael Faraday 1834 den Begriff "Ionen" (was griechisch "Die Wandernden" bedeutet). Die positiv geladenen Ionen bezeichnete Faraday als "Kationen", weil sie zur negativ geladenen Kathode streben, wogegen die negativ geladenen "Anionen" zur positiv geladenen Anode wandern.
Die Physiker verwenden seitdem den Begriff "Ionen" für Atome und Moleküle, die durch einen Überschuß oder Mangel an Elektronen negativ oder positiv geladen sind. Von Faraday stammen auch andere grundlegende Begriffe wie Elektrolyt, Elektrode, Kathode und Anode.

|
Svante Arrhenius (1859 - 1927) stellte 1887 die Ionentheorie auf. |
Dank Faraday war somit ein wesentlicher Vorgang bei der Elektrolyse geklärt. Offen blieb jedoch die Frage, wie es zur Entstehung der Ionen kommt. Sollte es der relativ geringen Energie des galvanischen Stroms tatsächlich gelingen, die Moleküle des Elektrolyten in Ionen aufzuspalten?
Der deutsche Physiker Rudolf Clausius bezweifelte dies. Er wagte 1857 die These, daß die Moleküle des Elektrolyten wenigstens zum Teil schon in Form von Ionen vorliegen müßten, bevor die elektrische Kraft auf sie einwirkt. Noch weiter ging der schwedische Wissenschaftler Svante Arrhenius: Seine 1887 aufgestellte "Ionentheorie" besagt, daß alle Stoffe, die in Lösung den Strom leiten, bei ihrer Auflösung in Wasser spontan in positiv oder negativ geladene Ionen zerfallen. Der gesamte Elektrolyt besteht demnach von vornherein aus Kationen bzw. Anionen.
Die Ionentheorie von Arrhenius war zunächst umstritten - bis der deutsche Physiker Walther Kossel 1916 herausfand, daß sämtliche Salze aus Ionen aufgebaut sind und ihre Lösung in Wasser lediglich die "elektrische Dissoziation" des von Natur aus vorhandenen Ionengitters bewirkt.
Seitdem wissen wir, das Wasser die Eigenschaft besitzt, Salze in ihre Ionen zu zerlegen. Wasserstoff und Metalle bilden in ihren Salzen stets Kationen, während Sauerstoff bzw. weitere Molekülteile in anionischer Form vorliegen.
Der Strom sorgt also lediglich dafür, daß die im Elektrolyten bereits vorhandenen Ionen je nach Art der Ladung zur einen oder zur anderen Elektrode wandern: So bewegen sich bei der Elektrolyse von Wasser die Kationen des Wasserstoffs (H+) zur Kathode als der negativ gepolten Elektrode. Sie beheben dort ihren Elektronenmangel aus der Stromquelle, wobei sich jeweils zwei H+ - Ionen in elektrisch neutrale Wasserstoff-Moleküle (H2) verwandeln. Gleichzeitig wandern die negativ geladenen Anionen des Sauerstoffmoleküls (O2-) zur Anode als der positiv gepolten Elektrode. Sie geben dort ihren Elektronenüberschuß an die Stromquelle ab und verwandeln sich in ein elektrisch neutrales Sauerstoff-Molekül (O2). Chemisch reines Wasser läßt sich allerdings kaum elektrolysieren, da die Ionenkonzentration zu gering ist. Man muß es deshalb durch Zugabe von Schwefelsäure oder Kalilauge erst leitfähig machen bzw. in eine Salzlösung verwandeln.
|
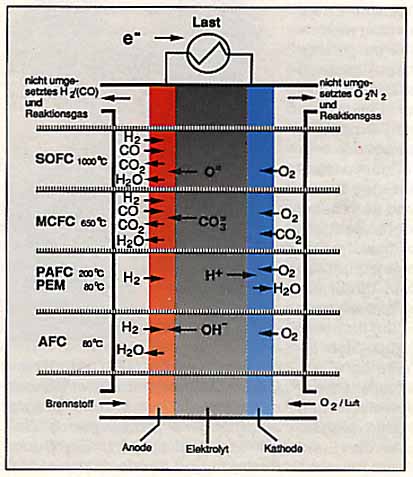
Je nach Art des verwendeten Elektrolyten verläuft bei den einzelnen Brennstoffzellen-Typen die Reaktion von Wasserstoff und Sauerstoff an den Elektroden unterschiedlich. |
Um die Elektrolyse umzukehren, so daß eine Brennstoffzelle daraus wird, bräuchte man eigentlich nur die Anode mit Wasserstoff und die Kathode mit Sauerstoff zu versorgen. Die entstehende elektrische Spannung zwischen den beiden Elektroden würde sich allerdings praktisch im selben Moment wieder über das Wasser bzw. den Elektrolyten ausgleichen, statt den "Umweg" über einen äußeren Stromkreis zu nehmen.
Man braucht also einen ganz besonderen Elektrolyten - eine Art Sperrschicht, die dafür sorgt, daß die durch die Ionenwanderung zwischen den Elektroden aufgebaute Spannung erhalten bleibt und über einen äußeren Stromkreis zwischen den beiden Elektroden genutzt werden kann.
Diese elektrolytische Sperrschicht ermöglicht es entweder den Sauerstoff-Ionen, den Weg zur Anode zu finden, oder umgekehrt den Wasserstoff-Ionen, die Wanderung zur Kathode anzutreten. Sie ist also entweder ein Sauerstoff-Ionen-Leiter oder ein Wasserstoff-Ionen-Leiter. Im zweiten Fall spricht man auch von einem Protonen-Leiter, da ein gewöhnliches Wasserstoff-Atom, dem sein einziges Elektron abhanden gekommen ist, nur noch aus einem Proton besteht.
In beiden Fällen reagieren die Ionen, die den Elektrolyten durchwandern, mit den Ionen der anderen Elektrode zu reinem Wasser. Zugleich entsteht an der Kathode ein Elektronenüberschuß, der sich durch Verbindung der beiden Elektroden als elektrische Spannung nutzen läßt.
Um aus der Brennstoffzelle eine leistungsfähige Stromquelle zu machen, müssen außerdem die Elektroden so gestaltet sein, daß sie den eingespeisten Wasserstoff und Sauerstoff hinreichend schnell heranführen und in Strom umsetzen können. Schließlich müssen auch noch Wasser und andere Reaktionsprodukte, die sich an den Elektroden niederschlagen oder den Elektrolyten verändern, zuverlässig abgeführt werden - abgesehen von zahlreichen weiteren technischen Problemen wie der Verhinderung einer allzu schnellen Korrosion der Zelle.